Lipid
Senin, 23 Januari 2012 | Ayun
| Laporan Praktikum Biokimia Umum | Hari/tanggal : Selasa/09 November 2010 Waktu : 08.00 – 11.00 WIB PJP : Waras Nurcholis Asisten : 1. Osy Yostia 2. Syaefuddin 3. Resti Siti Mutmainah |
LIPID
KELOMPOK 10
Randi Hadianta (G34090020)
Yovita Sari (G34090028)
Kurrataa’yun (G34090105)
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
2010
__________________________________________________________________________________
PENDAHULUAN
Lipid adalah senyawa organik berminyak atau berlemak yang tidak larut dalam air, dapat diekstrak dari sel dan jaringan oleh pelarut nonpolar, seperti kloroform dan eter. Asam lemak adalah komponen unit pembangun pada hampir semua lipid. Asam lemak adalah asam organik berantai panjang yang mempunyai atom karbon dari 4 sampai 24. Asam lemak memiliki gugus karboksil tunggal dan ekor hidrokarbon nonpolar yang panjang. Hal ini membuat kebanyakan lipid bersifat tidak larut dalam air dan tampak berminyak atau berlemak (Lehninger 1982).
Lipid secara umum dapat dibagi ke dalam dua kelas besar, yaitu lipid sederhana dan lipid kompleks. Yang termasuk lipid sederhana antara lain adalah: 1) trigliserida dari lemak atau minyak seperti ester asam lemak dan gliserol, contohnya adalah lemak babi, minyak jagung, minyak biji kapas, danbutter, 2) lilin yang merupakan ester asam lemak dari rantai panjang alkohol, contohnya adalahbeeswax, spermaceti, dan carnauba wax, dan 3) sterol yang didapat dari hidrogenasi parsial atau menyeluruh fenantrena, contohnya adalah kolesterol dan ergosterol (Scy Tech Encyclopedia 2008).
Lipid yang paling sederhana dan paling banyak mengandung asam lemak sebagai unit penyusunnya adalah triasilgliserol, juga sering disebut lemak, lemak netral, atau trigliserida. Jenis lipid ini merupakan contoh lipid yang paling sering dijumpai baik pada manusia, hewan, dan tumbuhan. Triasilgliserol adalah komponen utama dari lemak penyimpan atau depot lemak pada sel tumbuhan dan hewan, tetapi umumnya tidak dijumpai pada membran. Triasilgliserol adalah molekul hidrofobik nonpolar, karena molekul ini tidak mengandung muatan listrik atau gugus fungsional dengan polaritas tinggi (Lehninger 1982). Triasilgliserol terakumulasi di dalam beberapa area, seperti jaringan adiposa, dalam tubuh manusia dan biji tanaman, dan triasilgliserol ini mewakili bentuk penyimpanan energi. Lipid yang lebih kompleks berada dekat dan berhubungan dengan protein dalam membran sel dan partikel subselular. Jaringan yang lebih aktif mengandung lipid kompleks yang lebih banyak, contohnya adalah dalam otak, ginjal, paru-paru, dan darah yang mengandung konsentrasi fosfatida dalam jumlah tinggi pada mamalia (Scy Tech Encyclopedia 2008).
Lipid sebagai suatu senyawa memiliki sifat-sifat fisika dan kimia yang khas. Sifat-sifat fisika lipid antara lain terdapat pada warna, bau, kelarutan, polimorfisme, titik didih, dan indeks bias. Sifat-sifat kimia lipid meliputi reaksi-reaksi hidrolisis, oksidasi, dan esterifikasi. Zat warna dalam minyak terdiri dari zat warna alami dan hasil degradasi zat warna alami. Zat warna alami misalnya a dan ß karoten, santofil, klorofil, dan antosianin. Zat warna ini menyebabkan minyak berwarna kuning, kuning kecoklatan, kehijau-hijauan, dan kemerah-merahan (Winarno 1992).
Lemak atau bahan berlemak seperti lemak sapi, lemak babi, mentega, krim, susu bubuk, mempunyai bau seperti bau ikan yang sudah basi. Bau minyak alami berasal dari hasil urai asam-asam lemak atau komponen lain yang larut dalam minyak, seperti minyak sawit mempunyai bau yang khas karena adanya karoten (Montgomery et al 1993).
Kelarutan suatu zat dalam suatu pelarut ditentukan oleh kepolaran zat dan pelarut tersebut. Minyak dan lemak tidak larut dalam air, sedikit larut dalam alkohol, dan larut sempurna dalam kloroform. Sifat kelarutan minyak dan lemak digunakan untuk memisahkan minyak dari bahan yang mengandung minyak. Asam lemak rantai pendek dapat larut dalam air. Semakin panjang rantai asam lemak kelarutan dalam air semakin berkurang, asam lemak tidak jenuh lebih mudah larut dalam pelarut organik dibandingkan dengan asam lemak jenuh (Poedjiadi 1994).
TUJUAN
Praktikum ini bertujuan untuk mempelajari dan membandingkan sifat-sifat lipid melalui beberapa uji kualitatif untuk beberapa macam sampel lipid seperti minyak kelapa, lemak hewan, mentega, margarin, gliserol, asam palmitat dan asam stearat.
ALAT DAN BAHAN
Alat yang digunakan pada praktikum reaksi uji protein ini adalah tabung reaksi, pipet tetes, pipet volumetrik 5 mL, alat pengaduk, penangas air, labu erlenmeyer 100 mL, kertas saring, pembakar spiritus, dan sumbat karet. Sementara, bahan-bahan yang digunakan dalam praktikum ini adalah air, eter, kloroform, alkohol panas, alkohol dingin, alkali, asam encer, minyak kelapa, lemak hewan, mentega, margarin, gliserol, asam stearat, asam oleat, Kristal KHSO4, pereaksi Iod Hubl, HCl pekat, serbuk CaCO3, H2SO4, kolesterol, dan asam asetat anhidrat.
PROSEDUR PERCOBAAN
Uji kelarutan dilakukan dengan memasukkan 2 ml pereaksi ke dalam tabung reaksi lalu membubuhkan sedikit bahan percobaan kedalamnya. Tabung dikocok dan amati kelarutannya. Bahan pelarut yang digunakan adalah air, eter, kloroform, alkohol panas, alkohol dingin alkali, dan asam encer. Sementara bahan-bahan percobaan yang digunakan adalah minyak kelapa, lemak hewan, mentega, margarine, mentega, gliserol, dan asam stearat.
Uji Akrolein dilakukan dengan memasukkan sedikit Kristal KHSO4 ke dalam tabung lalu dibubuhkan3-4 tetes bahan percobaan. Tabung dipanaskan langsung diatas api dan asap akrolein yang muncul diperhatikan. Kemudian dibandingkan bau akrolein dengan bau SO2 yang terbang dari karbohidrat yang dipanaskan. Bahan uji yang digunakan adalah minyak kelapa, lemak hewan, gliserol, dan asam stearat.
Uji Ketidakjenuhan dilakukan dengan memasukkan 1 mL bahan percobaan ke dalam tabung reaksi lalu ditambahkan kloroform sebanyak 1 mL dan dikocok hingga larut. Kemudian Iod Hubl dibubuhkan sedikit demi sedikit sambil dikocok dan diamati perubahannya. Bahan-bahan yang diuji adalah minyak kelapa, minyak kelapa tengik, lemak hewan, mentega, margarin, dan asam oleat.
Uji Ketengikan dilakukan dengan memasukkan 5 ml bahan percobaan dan 5 ml HCL pekat kedalam labu Erlenmeyer 100 mL. Sebelumnya telah disediakan kertas floroglusinol dan sumbat karet. Serbuk CaCO3 dimasukkan ke dalam labung Erlenmeyer dan segera ditutup dengan sumbu karet, dengan posisi menjepit kertas floroglusinol yang dimasukkan tegak lurus ke dalam labu erlenmeyer menyentuh bahan percobaan. Kerta floroglusinol dibiarkan selama 10 -20 menit. Perubahan warna yang terjadi pada kertas diamati. Bahan yang diujikan adalah minyak kelapa tengik, minyak kelapa, lemak hewan dan mentega.
Uji Salkowski dilakukan dengan melarutkan beberapa milgram kolesterol dan 3 ml kloroform pada tabung reaksi. Selanjutnya ditambahkan asam sulfat pekat dengan volume yang sama, lalu tabung dikocok perlahan dan diamati perubahan warnanya.
Kedalam larutan kolesterol dan kloroform( hasil percobaan salkowski) ditambahkan 10 tetes asam asetat anhidrat dan 2 tetes asam sulfat pekat. Dikocok perlahan dibiarkan beberapa menit.
HASIL PENGAMATAN
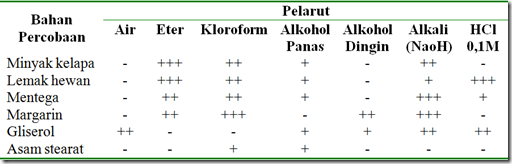
Tabel 1. Hasil uji kelarutan lipid
Gambar 1. Hasil uji kelarutan beberapa macam lipid pada air.
Gambar 2. Hasil uji kelarutan beberapa macam lipid pada alkohol dingin
Gambar 3. Hasil uji kelarutan beberapa macam lipid pada alkohol panas
Gambar 4. Hasil uji kelarutan beberapa macam lipid pada eter
Tabel 2. Uji Akrolein
| Nama Bahan | Pengamatan | Keterangan |
| Minyak kelapa | + | Bau SO2 |
| Lemak hewan | ++ | Bau akrolein |
| Gliserol | +++ | Bau akrolein |
| Asam stearat | ++ | Bau ekrolein |
| Ket : | + : Terdapat asap putih - : Tidak terdapat asap putih |
Tabel 3.Uji Ketidakjenuhan
| Nama Bahan | Pengamatan | Keterangan |
| Minyak kelapa | Kuning-merah-kuning | Tidak jenuh |
| Lemak hewan | Kuning-merah | Jenuh |
| Minyak kelapa tengik | Kuning-merah | Jenuh |
| Mentega | Kuning-merah-kuning | Tidak jenuh |
| Margarin | Kuning-merah-kuning | Tidak jenuh |
| Asam oleat | Kuning-merah-kuning | Tidak jenuh |
Gambar 5. Uji ketidakjenuhan pada minyak hewan, lemak hewan, minyak kelapa tengik, mentega, margarin, dan asam oleat berturut-turut dari kiri ke kanan.
Tabel 4. Uji Ketengikan
| Nama bahan | Pengamatan | Keterangan |
| Minyak kelapa tengik | +++ | Merah muda |
| Minyak kelapa | +++ | Merah muda |
| Lemak hewan | + | Jingga pudar |
| Mentega | ++ | Jingga terang |
| Ket : | + : Terjadi ketengikan - : Tidak terjadi ketengikan |
Tabel 5. Uji Salkowski
| Nama bahan | Perubahan Warna | Hasil uji |
| Kolesterol + (Kloroform dan H2SO4) | Degradasi 3 warna, merah pekat, jingga dan kuning | + |
| Ket : | + : Terdapat kolesterol - : Tidak terdapat kolesterol |
Gambar 7. Uji Salkowski dengan kloroform dan H2SO4.
Tabel 6. Uji Lieberman Buchard untuk kolesterol
| Nama bahan | Perubahan Warna | Hasil uji |
| Kolesterol + (Kloroform dan H2SO4) + asam asetat | Degradasi 4 warna, hijau pekat, merah pekat, jingga dan kuning | + |
| Ket: | + : Mengandung kolesterol - : Tidak mengandung kolesterol |
Gambar 8. Uji Lieberman Buchard untuk kolesterol
DAFTAR PUSTAKA
Lehninger AL. 1982. Dasar-Dasar Biokimia Jilid I (terjemahan). Jakarta: Erlangga.
Montgomery et al. 1993. Biochemistry: A Case Oriented Approach. The CV Mosby Company, St. Louis.
Poedjiadi Anna. 1994. Dasar-Dasar Biokimia. Jakarta: Penerbit UI-Press.
Scy Tech Encyclopedia. 2008. Lipid. (terhubung berkala). http://www.answers.com /library/Sci%252DTech %20 Encyclopedia-cid- 47286. html. (10 November 2010).
Winarno, F.G. 1992. Kimia Pangan dan Gizi. Jakarta: PT. Gramedia.

![clip_image002[5] clip_image002[5]](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEj3Hk6EZU4MHj3y0hVj48-fe_95-8x1hYqEOuO9CLB5wb3gaUXpYRexcNOXsnqffNqYKMSuje9oc5F14kZrFyQQkMEjDCuA111azHjX1-DG80NKLJLJMPErevJiMve_mbMBhSQ6XqBteS0/?imgmax=800)





0 comments:
Posting Komentar